3′-એમિનો-2′-હાઈડ્રોક્સી-[1,1'-બાયફેની]-3-કાર્બોક્સિલિક એસિડ
3′-એમિનો-2′-હાઈડ્રોક્સી-[1,1'-બાયફેની]-3-કાર્બોક્સિલિક એસિડ
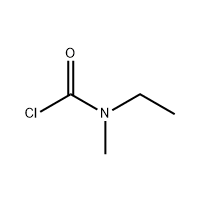
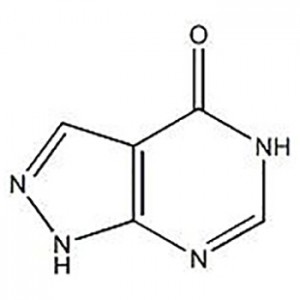
3'-Amino-2'-hydroxy-[1,1'-bipheny]-3-કાર્બોક્સિલિક એસિડનો ઉપયોગ એલ્ટ્રોમ્બોપેગના મધ્યવર્તી તરીકે થાય છે.
એલ્ટ્રોમ્બોપેગ, યુકેમાં ગ્લેક્સોસ્મિથક્લાઇન (જીએસકે) દ્વારા વિકસિત અને બાદમાં સ્વિટ્ઝર્લેન્ડમાં નોવાર્ટિસ સાથે સંયુક્ત રીતે વિકસિત, વિશ્વમાં પ્રથમ અને એકમાત્ર માન્ય નાના અણુ નોન પેપ્ટાઇડ TPO રીસેપ્ટર એગોનિસ્ટ છે.એલ્ટ્રોમ્બોપૅગને 2008 માં યુએસ એફડીએ દ્વારા આઇડિયોપેથિક થ્રોમ્બોસાયટોપેનિક પુરપુરા (ITP) ની સારવાર માટે અને 2014 માં ગંભીર એપ્લાસ્ટિક એનિમિયા (AA) ની સારવાર માટે મંજૂરી આપવામાં આવી હતી.તાજેતરના 30 વર્ષોમાં એએની સારવાર માટે યુએસ એફડીએ દ્વારા મંજૂર કરાયેલી તે પ્રથમ દવા પણ છે.
ડિસેમ્બર 2012માં, યુએસ એફડીએ એ ક્રોનિક હેપેટાઇટિસ C (CHC) ધરાવતા દર્દીઓમાં થ્રોમ્બોસાયટોપેનિયાની સારવાર માટે એલ્ટ્રોમ્બોપેગને મંજૂરી આપી હતી, જેથી પ્લેટલેટની ઓછી સંખ્યાને કારણે નબળા પૂર્વસૂચન ધરાવતા હેપેટાઇટિસ સીના દર્દીઓ યકૃતના રોગો માટે ઇન્ટરફેરોન આધારિત માનક ઉપચાર શરૂ કરી શકે અને જાળવી શકે.ફેબ્રુઆરી 3,2014 ના રોજ, ગ્લેક્સોસ્મિથક્લાઈને જાહેરાત કરી હતી કે એફડીએ એ ગંભીર કેમિકલબુક એપ્લાસ્ટિક એનિમિયા (SAA) ધરાવતા દર્દીઓમાં હિમોપેનિયાની સારવાર માટે એલ્ટ્રોમ્બોપેગની સફળતાપૂર્વક સારવારની દવાની લાયકાત મંજૂર કરી છે જેમણે ઇમ્યુનોથેરાપીને સંપૂર્ણ પ્રતિસાદ આપ્યો નથી.24 ઓગસ્ટ, 2015 ના રોજ, યુએસ એફડીએ એ ક્રોનિક ઇમ્યુન થ્રોમ્બોસાયટોપેનિયા (ITP) ધરાવતા પુખ્ત વયના લોકો અને 1 વર્ષ અને તેથી વધુ ઉંમરના બાળકોમાં થ્રોમ્બોસાયટોપેનિઆની સારવાર માટે એલ્ટ્રોમ્બોપેગને મંજૂરી આપી હતી, જેમને કોર્ટીકોસ્ટેરોઇડ્સ, ઇમ્યુનોગ્લોબ્યુલિન અથવા સ્પ્લેનેક્ટોમી માટે અપૂરતો પ્રતિભાવ છે.જાન્યુઆરી 4,2018 ના રોજ, એલ્ટ્રોમ્બોપેગને પ્રાથમિક રોગપ્રતિકારક થ્રોમ્બોસાયટોપેનિયા (ITP) ની સારવાર માટે ચીનમાં સૂચિબદ્ધ કરવાની મંજૂરી આપવામાં આવી હતી.


![3′-Amino-2′-hydroxy-[1,1'-bipheny]-3-કાર્બોક્સિલિક એસિડ ફીચર્ડ ઈમેજ](http://cdn.globalso.com/jindunchem-med/image351.png)
![3′-એમિનો-2′-હાઈડ્રોક્સી-[1,1'-બાયફેની]-3-કાર્બોક્સિલિક એસિડ](http://cdn.globalso.com/jindunchem-med/image351-300x300.png)
![6-ટેટ્રા-ઓ-એક્ટેઇલ-1-સી-[4-ક્લોરો-3-[[4-[[(3S)-ટેટ્રાહાઇડ્રોફુ-રેન-3-yl]ઓક્સી]ફિનાઇલ]](http://cdn.globalso.com/jindunchem-med/0ecf55f0-300x300.jpg)